编者按:本文转载自奇点网,微信公众号(geekheal_com),e科网经授权转载。
造物主在创造生命、设计遗传信息的时候,绝对想到了所有生命都会经历吃不饱和能吃撑两个阶段。
但她没想到的应该是,数十万年间一直处于饥寒交迫状态的人类,突然在短短几十年间就过上了顿顿能吃撑的好日子。
进入20世纪之后,被肥胖症、糖尿病和高血压等代谢疾病困扰的人类,一开始始终不明白:为什么日子变得好过了,身体却不如从前了?
1962年,人类遗传学家James Neel一声惊雷,提出“节俭基因”假说(A “Thrifty” Genotype)[1]。

他说,在远古的时候啊,人类的祖先那真是靠天吃饭啊,因为四季和雨水的变化,食物的供应都是周期性的。很可能出现饱餐一顿之后,后面的几百顿都吃不饱了。
于是,那些因基因变异,变得消化吸收好,能最大限度把食物转化成脂肪储存起来的远古人类,在食物充足的时候,能快速增肥,以应对随时到来的食物缺乏时期。Neel认为,“节俭基因”就在这批人体内出现了,这在当时环境下是很有优势的。
但是在现如今这个顿顿都能吃撑的年代,“节俭基因”就顺理成章地成了肥胖症、糖尿病和高血压等疾病的罪魁祸首。
不过,从去年发表在《新英格兰医学期刊》上的195个国家肥胖数据来看,2015年全球肥胖人数大概在8亿左右,成人肥胖率最高的埃及,也只有35.3%[2]。绝大多数人还是不胖。这又是为什么?
当然,“造物主给了我们易肥胖的基因,到底胖不胖也得看环境”。
这当然是一方面原因,不过今天我们要说的是另一个有趣的原因。
近日,著名期刊《细胞代谢》杂志以封面论文的形式,发表了厦门大学林圣彩教授和林舒勇副教授研究团队的重要研究成果[3],因为他们发现了一个名叫Aida的“浪费基因”(“wasteful” gene)。该论文的共同第一作者为罗辉和姜鸣。

图:《细胞代谢》杂志封面。图中女性名叫Aida,是古埃塞俄比亚公主。图片借Aida与埃及将军Radames爱情故事,比喻Aida基因抑制脂肪吸收的机制
这个浪费基因啊,她很奇特,正常情况下,她是限制小肠吸收脂肪的。这跟“节俭基因”一比,可不是显得很浪费么。
根据她这一特定,我很快就想到一句话,“酒肉穿肠过,佛祖心中留”。于是,干脆叫她“酒肉穿肠过”基因了。
Aida这个基因最早是林圣彩教授团队与清华大学孟安明院士团队合作鉴定和命名的[4],当时对Aida的具体功能还不是很清楚。
当林圣彩团队从小鼠体内去掉Aida基因后,他们发现与Aida基因还在的小鼠比,没Aida基因的小鼠胖的像充了气一样。
看来Aida基因是防止变胖的啊~
于是林圣彩和林舒勇团队就围绕没有Aida基因的易胖小耗子研究了10年。
他们发现,食物中脂肪在小肠吸内的收效率是个体易肥胖的一个主要决定因素。而Aida基因编码的AIDA蛋白质就是控制整个过程的。
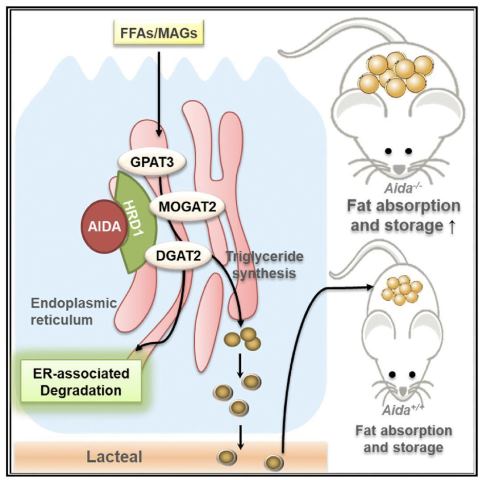
图:AIDA蛋白的作用机制
也许你可能不知道,我们吃到肚子里的脂肪,经过胃的简单消化之后,就进入小肠被进一步消化成能被小肠细胞吸收的物质,紧接着就被小肠上皮细胞吸收[5];然后小肠的上皮细胞又重新把它们变成便于运输的脂肪类型,分泌给淋巴,最后脂肪就通过血管输送到全身被各个器官利用或储存[6]。
Neel提出的“节俭基因”假说设计的部分基因可能也参与了上述过程。
林教授团队发现,在没有Aida基因小鼠体内,小肠细胞中与脂肪合成相关酶大量表达,加快脂肪的合成,这样一来小肠细胞就腾出空间继续从小肠里吸收脂肪的代谢产物了。这就间接的促进小肠对脂肪的吸收。
如果要深究背后的原因的话,那就是这样的。AIDA这个蛋白原本是通过内质网降解途径(ERAD)促进小肠细胞内脂肪合成酶降解的,把她搞没了,小肠细胞就只能疯狂的吸收脂肪了。
如果再啰嗦一下,就是说小肠细胞你可以从肠道中吸收原料合成脂肪,但是你得有个度,这个度就是由AIDA控制。AIDA说不要合成了,那小肠细胞的合成和吸收就都变慢,甚至停止了。
造物主想的真是周到,给哺乳动物一套高效的脂肪吸收系统,同时还给了一个限制调节的方法。
所以那些很容易就胖的,Aida基因是不是坏了?那些吃啥都胖不起来的,Aida基因是不是过度活跃了?
参考资料:
[1]. Neel J V. Diabetes mellitus: a “thrifty” genotype rendered detrimental by “progress”?[J]. American journal of human genetics, 1962, 14(4): 353.
[2]. GBD 2015 Obesity Collaborators. Health effects of overweight and obesity in 195 countries over 25 years[J]. New England Journal of Medicine, 2017, 377(1): 13-27.
[3]. Luo H, Jiang M, Lian G, et al. AIDA Selectively Mediates Downregulation of Fat Synthesis Enzymes by ERAD to Retard Intestinal Fat Absorption and Prevent Obesity[J]. Cell Metabolism, 2018, 27(4): 843-853. e6.
[4]. Rui Y, Xu Z, Xiong B, et al. A beta-catenin-independent dorsalization pathway activated by Axin/JNK signaling and antagonized by Aida[J]. Developmental Cell, 2007, 13(2): 268-282.
[5]. Tso P, Nauli A M, Lo C, et al. Enterocyte fatty acid uptake and intestinal fatty acid-binding protein[J]. Biochemical Society Transactions, 2004, 32(1): 75-78.
[6]. Dash S, Xiao C, Morgantini C, et al. New Insights into the Regulation of Chylomicron Production[J]. Annual Review of Nutrition, 2015, 35(1): 265-294.
如若转载,请注明e科网。
如果你有好文章想发表or科研成果想展示推广,可以联系我们或免费注册拥有自己的主页
- 厦门大学
- 浪费基因


 我要投稿
我要投稿