响应型上转换纳米组装体用于pH激活近红外激发的深部肿瘤光动力治疗
作者:Fangyuan Li, Yang Du, Jianan Liu, Heng Sun, Jin Wang, Ruiqing Li, Dokyoon Kim, Taeghwan Hyeon, Daishun Ling
●
2018-07-24 17:16:22
一、研究背景
光动力治疗具有非侵入和时空响应等优势,因此已被开发应用于肿瘤的临床治疗。然而,传统光动力治疗所用到的可见光光源,对组织的穿透能力有限,无法用于治疗深部肿瘤。并且,现有的小分子光敏剂缺乏肿瘤部位选择性,因此患者在日光或强光照射后可能出现皮肤光过敏的现象,加重了患者的负担。对此,本文通过将上转换纳米粒子和连接光敏剂分子的pH响应高分子进行组装,开发了一种肿瘤微环境响应的上转换纳米组装体用于深部肿瘤的光动力治疗。
二、研究亮点与特色
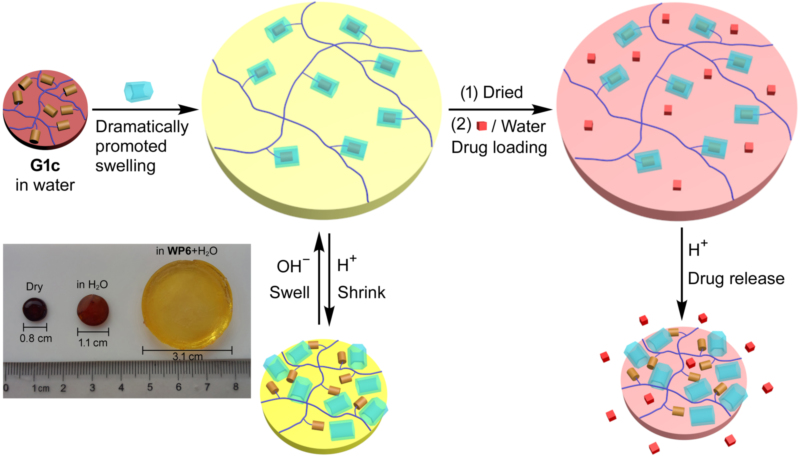
(1) 上转换纳米组装体在正常生理pH条件下(pH~7.4),表面电位显负价,光敏剂聚集在纳米组装体中呈淬灭状态不具有光活性。一旦纳米组装体进入到肿瘤微酸环境中(pH~6.5),纳米组装体表面电位由负价变为正价,更易吸附于带有负价的细胞膜表面而进入肿瘤细胞。同时组装体内部静电斥力增强,纳米组装体在微酸环境中逐渐膨胀,导致光敏剂分子间的距离增大,逐渐恢复光敏剂的光活性。在肿瘤胞内pH条件下(pH~5.5),纳米组装体彻底解离,彻底激活光敏剂分子,实现肿瘤微环境可控的光动力治疗。
(2) 上转换纳米粒子通过吸收组织穿透力更强的近红外光发射出红光激发活化的光敏剂分子,同时上转换发光成像实时指导治疗,实现成像指导的深部肿瘤光动力治疗。
三、预期社会与经济效益
解决了目前光动力治疗肿瘤的两大难题:(1)肿瘤选择性低,存在光毒性等副作用;(2)无法用来治疗深部肿瘤。为开发新一代诊疗一体光动力治疗药物,提供理论依据。
四、下一步工作
对响应型上转换纳米组装体进行体内毒理学评价,为未来的临床转化提供理论指导依据。
下载作者原文
文章二维码:
如若转载,请注明e科网。
产品使用建议和意见可以联系小编进行优化处理:QQ:252188815、微信:13581664931
-
光动力治疗;上转换纳米粒子;pH响应;纳米组装体;诊疗一体化。
Responsive Assembly of Upconversion Nanoparticles for pH‐Activated and Near‐Infrared‐Triggered Photodynamic Therapy of Deep Tumo
作者:Fangyuan Li, Yang Du, Jianan Liu, Heng Sun, Jin Wang, Ruiqing Li, Dokyoon Kim, Taeghwan Hyeon, Daishun Ling
●
2018-07-24 17:16:22
导语
Upconversion nanoparticle (UCNP)‐mediated photodynamic therapy has shown great effectiveness in increasing the tissue‐penetration depth of light to combat deep‐seated tumors. However, the inevitable phototoxicity to normal tissues resulting from the lack of tumor selectivity remains as a major challenge. Here, the development of tumor‐pH‐sensitive photodynamic nanoagents (PPNs) comprised of self‐assembled photosensitizers grafted pH‐responsive polymeric ligands and UCNPs is reported. Under neutral pH conditions, photosensitizers aggregated in the PPNs are self‐quenched; however, upon entry into a tumor microenvironment with lower pH, the PPNs not only exhibit enhanced tumor‐cell internalization due to charge reversal but also are further disassembled into well‐dispersed nanoparticles in the endo/lysosomes of tumor cells, enabling the efficient activation of photosensitizers. The results demonstrate the attractive properties of both UCNP‐mediated deep‐tissue penetration of light and high therapeutic selectivity in vitro and in vivo.
文章全文链接
如若转载,请注明e科网。
如果你有好文章想发表or科研成果想展示推广,可以联系我们或免费注册拥有自己的主页


 我要投稿
我要投稿