多亏这些谦逊的水母,更加安全地绘制人体细胞的激光或将很快应用于临床。
常规激光,比如逗小猫的指示器是通过让相同的光子在一个腔体内弹跳并散射从而产生光。若将其扩大规模则需要大量能量支撑。
另一种类型的激光叫作极化声子激光,通过在受刺激的分子中间来回传递光子发挥作用。与常规激光不同,这种光子在缩小成为激光之前,会在设备内被反复释放和重新吸收。它们比常规激光耗用的能量更少,因此在理论上可以形成更加有效的光通信,或是对活体组织破坏性较小的医疗激光。
然而这里也有一个问题:大多数极化声子激光只能在极端低温下更好地发挥作用。在室温下操作产生光的分子可以让它们变得更加实用。但是可以在室温下发挥作用的极少数材料光散射分子却过于接近,因此会相互干扰而不产生激光。
近日,一个由英德科学家组成的研究团队在最近出版的《科学·进展》杂志上发表论文称,他们首次将水母体内的荧光蛋白基因插入大肠杆菌基因组,利用转基因大肠杆菌产出了增强型绿色荧光蛋白(eGFP)并用来产生激光。研究人员指出,这一突破代表着极化激元激光领域的重大进步,其效率和光密度都比普通激光高得多,有望为研究量子物理学和光学计算开辟新途径。
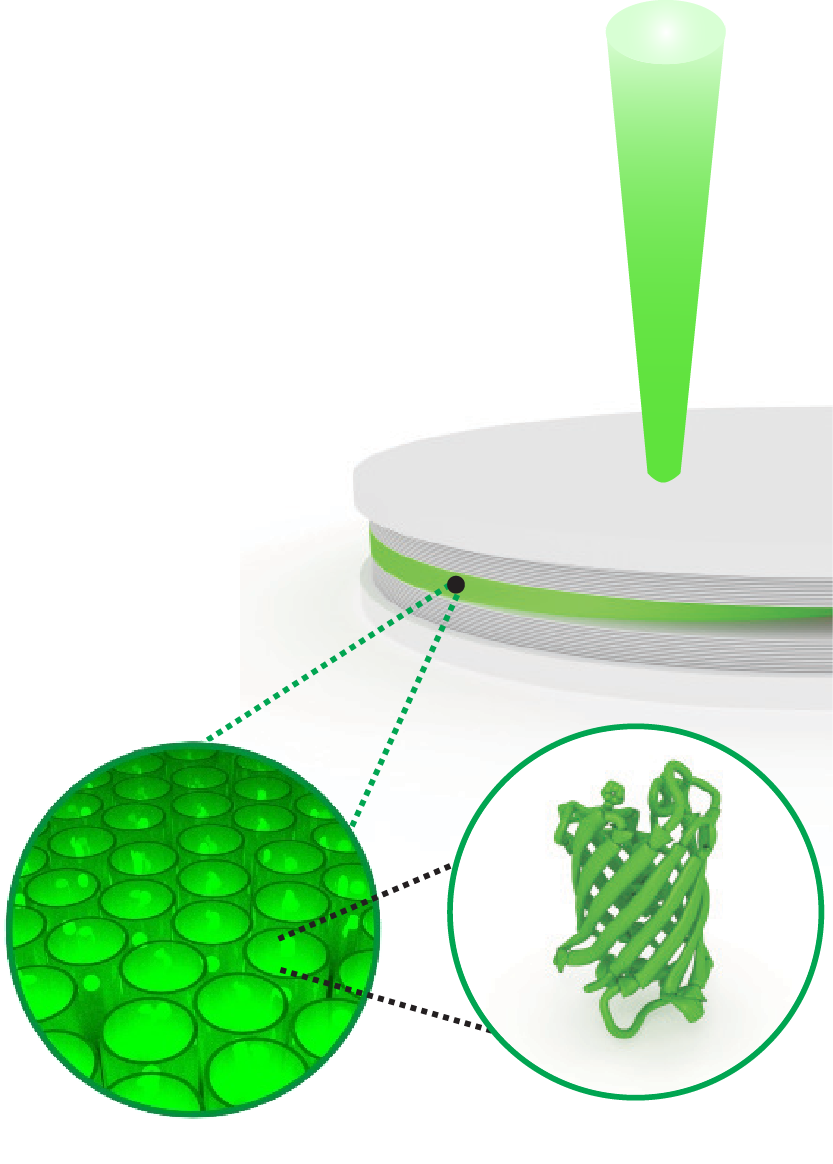
图:绿色荧光蛋白极化激元激光原理示意图:将活细胞产生的绿色荧光蛋白填充在微光腔中制成一层薄膜,光和电子能量混合产生准粒子。
研究人员把转基因大肠杆菌产生的eGFP填充在许多光微腔里,作为一种“光泵”,能以纳秒速度发出闪光,使整个系统达到产生激光所需的能量。“光泵”能在达到激发阈值后,给设备注入更多能量以产生传统激光。该激光发明人之一、苏格兰圣安德鲁大学物理与天文学院教授Malte Gather说,皮秒脉冲的能量更合适,但制造起来要比纳秒脉冲难1000倍,他们的做法简化了很多制造工序。

Malte Gather还指出,新方法的一个关键优点是,蛋白质分子的发光部分被一种纳米大小的圆柱形外壳保护着,让它们彼此间不会互相干扰,分子结构很适合在高亮度下工作,更容易发出激光。但目前的激发阈值还太高,今后经过改进,最终可让极化激元激光器的激发阈值比传统激光器低得多,这样效率会更高,发光更致密。
文章链接:
Christof P. Dietrich, et al, "An exciton-polariton laser based on biologically produced fluorescent protein," Science Advances 19 Aug 2016:Vol. 2, no. 8, e1600666, DOI: 10.1126/sciadv.1600666
(本文文字来源:科技日报;)
如若转载,请注明e科网。
如果你有好文章想发表or科研成果想展示推广,可以联系我们或免费注册拥有自己的主页
- 极化激元激光


 我要投稿
我要投稿